Lv et al. (2021)を参考に作成
【結論】脂肪由来幹細胞治療は老化関連疾患の改善に期待できる再生医療
1. 脂肪由来幹細胞(ADSCs)とは:皮下脂肪から採取できる多能性幹細胞で、採取が容易で安全性が高い
2. 老化との関連性:ADSCsは代謝恒常性を調節し、ミトコンドリアのオートファジーを促進することで老化を遅延させる可能性
3. 臨床的有効性:変形性膝関節症に対する大規模臨床試験で疼痛軽減・機能改善効果が実証(Lee et al., 2019; Lee et al., 2023)
4. 多様な治療可能性:心血管保護、組織修復、免疫調節など、複数の作用機序を持つ包括的な治療法
5. 安全性の確立:Phase III臨床試験で重篤な副作用なく安全性が確認されている
6. 今後の展望:老化に伴う様々な疾患への応用が期待され、アンチエイジング医療の新たな選択肢として注目
「膝の痛みが年齢とともにひどくなってきた…」「老化による体の衰えを何とかしたい…」―そんなお悩みをお持ちではありませんか?
近年、再生医療の分野で注目を集めているのが脂肪由来幹細胞(Adipose-Derived Stem Cells: ADSCs)を用いた治療法です。皮下脂肪から容易に採取でき、組織修復・炎症抑制・代謝調節など多彩な作用を持つADSCsは、老化に伴う様々な疾患の改善に期待が寄せられています。
脂肪由来幹細胞治療の科学的根拠
- 変形性膝関節症への有効性:Phase III臨床試験(261例)で疼痛VASが25.2点改善(プラセボ群15.5点 p=0.004)(Lee et al., 2023)
- 機能改善効果:WOMAC総スコアが21.7点改善(プラセボ群14.3点 p=0.002)(Lee et al., 2023)
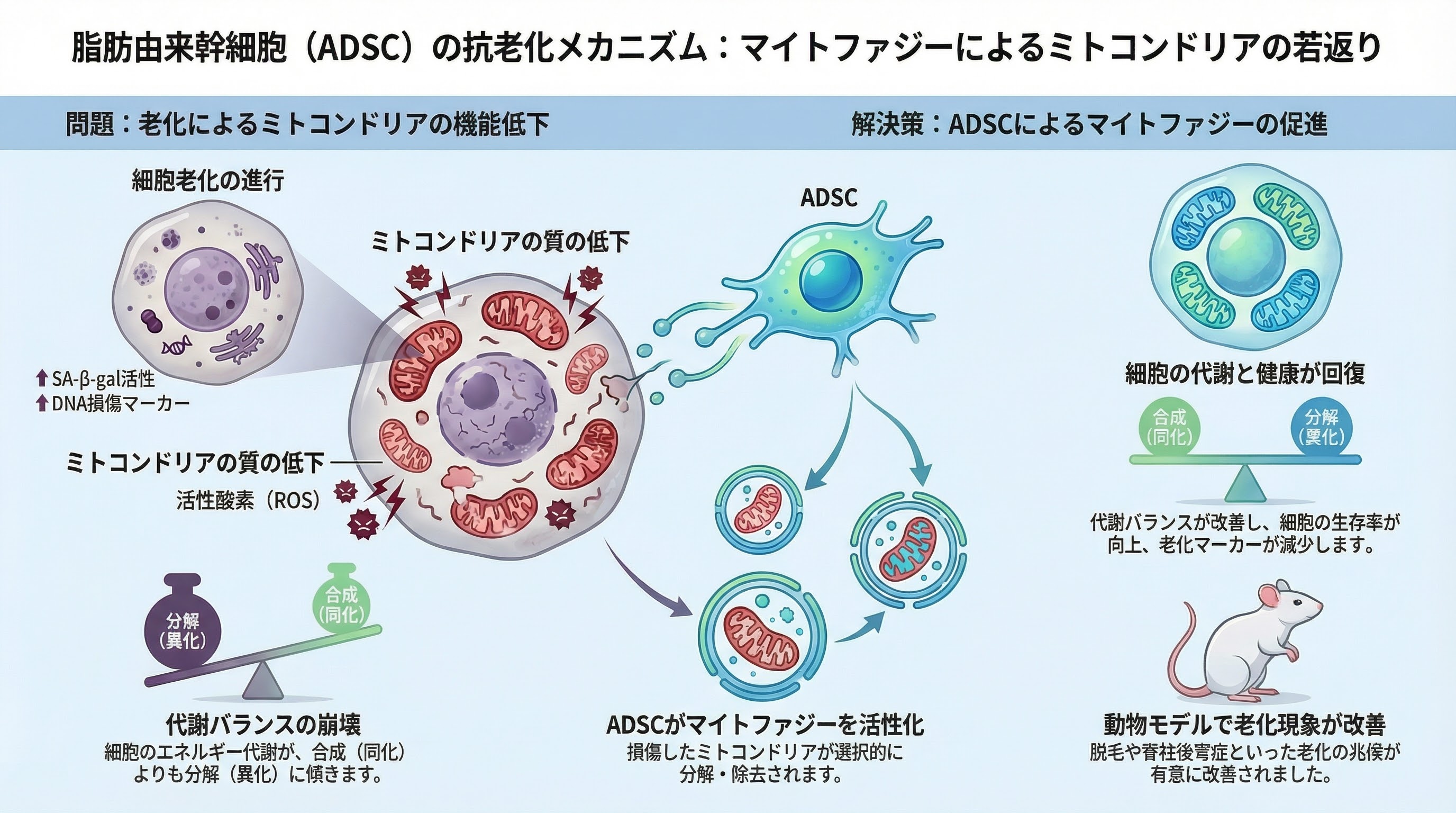
- 老化遅延効果:ミトファジー促進により代謝恒常性を調節し老化を遅延(Lv et al., 2021)
- 安全性の確立:重篤な治療関連有害事象なし(Lee et al., 2019; Lee et al., 2023)
- 長期効果の持続:5年間のフォローアップで効果と安全性を確認(Kim et al., 2022)
- → 科学的根拠に基づいた安全で有効な治療法として確立
本記事では、再生医療の専門的視点から、エビデンスに基づいて脂肪由来幹細胞治療の仕組み・効果・応用と、老化関連疾患への治療可能性を詳しく解説します。
この記事で分かること
・脂肪由来幹細胞とは:特性・採取方法・作用機序
・老化との関連性:代謝調節・ミトファジー促進による老化遅延メカニズム
・臨床的有効性:変形性膝関節症などへの治療効果
・多様な治療可能性:心血管保護・組織修復・免疫調節
・安全性と副作用:大規模臨床試験による検証結果
・よくある質問:患者さんの疑問に専門医が回答
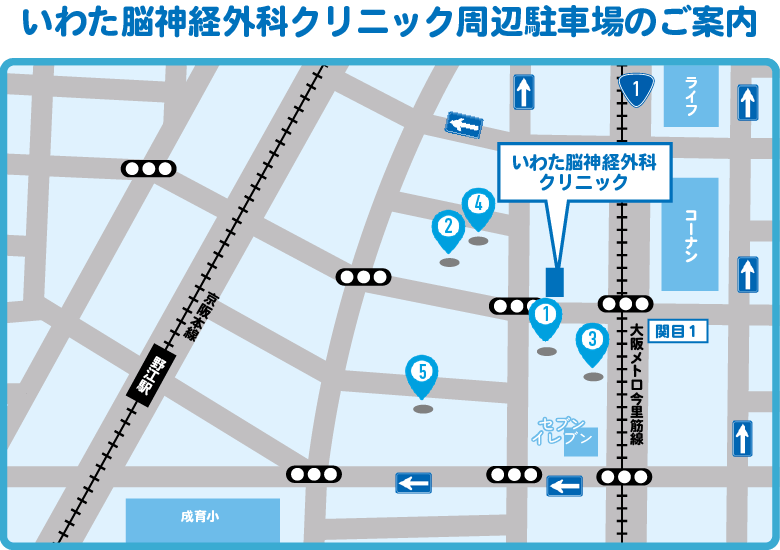
大阪で再生医療・幹細胞治療の相談なら、いわた脳神経外科クリニックへどうぞ。ご予約は、下記から可能です。
目次
1. 脂肪由来幹細胞とは
1-1. 脂肪由来幹細胞の定義と特徴
脂肪由来幹細胞(Adipose-Derived Stem Cells: ADSCs)は、皮下脂肪組織から採取される間葉系幹細胞の一種です。脂肪組織は豊富で容易にアクセス可能な幹細胞源として、再生医療の分野で大きな注目を集めています(Gimble et al., 2007)。
脂肪由来幹細胞の特徴
- 採取の容易性:局所麻酔下での脂肪吸引により、低侵襲かつ安全に採取可能
- 豊富な細胞数:脂肪組織は間葉系幹細胞を骨髄の約500倍含有(Gimble et al., 2007)
- 多分化能:脂肪細胞・骨細胞・軟骨細胞・血管内皮細胞など多様な細胞へ分化可能
- パラクリン効果:成長因子・サイトカインを分泌し、組織修復・炎症抑制を促進
- 免疫調節作用:免疫反応を調整し、過剰な炎症を抑制
- 血管新生促進:VEGF(血管内皮成長因子)を分泌し、新たな血管形成を促進
1-2. 骨髄由来幹細胞との比較
| 比較項目 | 脂肪由来幹細胞(ADSCs) | 骨髄由来幹細胞(BMSCs) |
|---|---|---|
| 採取方法 | 局所麻酔下の脂肪吸引(低侵襲) | 全身麻酔下の骨髄穿刺(侵襲的) |
| 細胞数 | 非常に豊富(骨髄の約500倍) | 限定的 |
| 増殖能 | 高い増殖速度 | 増殖速度は遅い |
| 分化能 | 多分化能あり | 多分化能あり |
| 患者負担 | 軽度 | 中等度~重度 |
| 培養効率 | 高効率 | 低~中等度 |
※Gimble et al. (2007)より
1-3. 採取と培養のプロセス
臨床応用における脂肪由来幹細胞の調製は、以下のステップで行われます:
- 脂肪組織の採取:局所麻酔下で腹部や大腿部から脂肪吸引(約10-20ml)
- 酵素処理:コラゲナーゼなどの酵素で脂肪組織を消化
- 間質血管細胞画分(SVF)の分離:遠心分離により幹細胞を含むSVFを取得
- 細胞培養:培養液中で2-4週間培養し、細胞数を増やす(培養拡大)
- 品質管理:細胞の純度・生存率・分化能を確認
- 治療への応用:関節内注射や静脈内投与など、目的に応じた投与
自家移植と同種移植
- 自家移植:患者自身の脂肪組織から採取した幹細胞を使用。免疫拒絶反応のリスクが低く、臨床試験で主に採用
- 同種移植:他人(ドナー)の幹細胞を使用。大量生産が可能だが、免疫適合性の確認が必要
2. 幹細胞と老化のメカニズム
2-1. 老化とミトコンドリア機能不全
老化の根本的なメカニズムの一つとして、ミトコンドリアの機能不全が注目されています。ミトコンドリアは細胞のエネルギー産生を担う重要な小器官ですが、加齢とともに損傷が蓄積し、以下のような変化が生じます:
- 活性酸素種(ROS)の増加:ミトコンドリアから発生する活性酸素が細胞を損傷
- ATP産生の低下:エネルギー産生効率が低下し、細胞機能が衰える
- ミトコンドリアDNAの変異:遺伝子変異が蓄積し、機能不全が進行
- 代謝恒常性の破綻:糖・脂質代謝の異常が生じる
2-2. ミトファジーによる老化遅延
近年の研究により、脂肪由来幹細胞がミトファジー(ミトコンドリアのオートファジー)を促進することで老化を遅延させる可能性が示されています(Lv et al., 2021)。
ミトファジーとは
ミトファジーは、損傷したミトコンドリアを選択的に分解・除去し、新しいミトコンドリアに置き換える細胞内の品質管理システムです。このプロセスは以下のような効果をもたらします:
- 活性酸素の産生抑制:損傷ミトコンドリアを除去することでROSを減少
- 代謝機能の維持:健全なミトコンドリアにより代謝恒常性を保持
- 細胞老化の遅延:細胞機能を維持し、老化関連疾患を予防
- 炎症反応の抑制:損傷ミトコンドリア由来の炎症シグナルを減少
2-3. 脂肪由来幹細胞による代謝調節
Lv et al. (2021)の研究では、脂肪由来幹細胞が以下のメカニズムで代謝恒常性を調節し、老化を遅延させることが示されました:
| 作用機序 | 効果 | 老化への影響 |
|---|---|---|
| ミトファジーの促進 | 損傷ミトコンドリアの除去 | 活性酸素減少、細胞機能維持 |
| 代謝遺伝子の調節 | 糖・脂質代謝の改善 | 代謝疾患の予防 |
| 抗炎症作用 | 炎症性サイトカインの抑制 | 慢性炎症の軽減 |
| 抗酸化作用 | 酸化ストレスの軽減 | 細胞損傷の予防 |
| 組織修復促進 | 成長因子の分泌 | 組織の再生能力維持 |
※Lv et al. (2021)より
2-4. 老化関連疾患への応用可能性
ミトファジー促進と代謝調節作用により、脂肪由来幹細胞は以下のような老化関連疾患への治療応用が期待されています:
- 変形性関節症:軟骨の変性・炎症を抑制(後述の臨床試験で実証)
- 心血管疾患:血管新生促進・心筋保護作用(Gimble et al., 2007)
- 神経変性疾患:神経保護・抗炎症作用
- 代謝症候群:インスリン感受性改善・脂質代謝調節
- 皮膚老化:コラーゲン産生促進・組織修復
老化のメカニズムと幹細胞治療:
老化は単一の原因ではなく、ミトコンドリア機能不全・酸化ストレス・慢性炎症など複数の要因が複雑に絡み合って進行します。脂肪由来幹細胞は、ミトファジー促進による代謝調節を通じて、これらの老化メカニズムに多面的にアプローチできる可能性があります(Lv et al., 2021)。ただし、実際の臨床応用においては、疾患の種類や患者の状態に応じた適切な評価が必要です。
大阪で頭痛のことなら、いわた脳神経外科クリニックへどうぞ。ご予約は、下記から可能です。
3. 臨床的有効性:エビデンスに基づく治療効果
3-1. 変形性膝関節症に対する大規模臨床試験
変形性膝関節症は、加齢に伴う代表的な疾患であり、軟骨の変性・磨耗により疼痛・機能障害を引き起こします。Lee et al. (2023)によるPhase III多施設無作為化比較試験では、261例の患者を対象に脂肪由来幹細胞の有効性と安全性が検証されました。
Phase III臨床試験の概要(Lee et al., 2023)
- デザイン:多施設共同・二重盲検・無作為化・プラセボ対照試験
- 対象:Kellgren-Lawrence grade 3の症候性膝関節症患者261例
- 介入:自家培養拡大脂肪由来幹細胞の関節内単回注射(1億個の細胞)
- 主要評価項目:6ヶ月後のVAS疼痛スコアとWOMAC機能スコアの改善
- フォローアップ期間:6ヶ月(3ヶ月・6ヶ月時点で評価)
3-2. 主要評価項目の結果
| 評価項目 | ADMSC群(n=125) | 対照群(n=127) | p値 |
|---|---|---|---|
| VAS疼痛スコア改善(6ヶ月) | 25.2点 | 15.5点 | 0.004 |
| WOMAC総スコア改善(6ヶ月) | 21.7点 | 14.3点 | 0.002 |
| WOMAC疼痛スコア改善 | 有意に改善 | 改善 | <0.05 |
| WOMAC機能スコア改善 | 有意に改善 | 改善 | <0.05 |
| 臨床的重要改善達成率 | 有意に高い | 標準 | <0.05 |
※Lee et al. (2023)より。VAS: Visual Analog Scale(100mm)、WOMAC: Western Ontario and McMaster Universities Osteoarthritis Index
3-3. Phase IIb試験の結果(Lee et al., 2019)
同じ研究グループによるPhase IIb試験(140例)でも、同様の有効性が確認されています:
- VAS疼痛スコア:低用量群・高用量群ともに対照群と比較して有意に改善
- WOMAC総スコア:投与6ヶ月後に有意な改善を示し、効果は12ヶ月まで持続
- 用量反応関係:高用量(1億個)群でより顕著な改善傾向
- MRI所見:一部の患者で軟骨の質的改善を示唆する所見
3-4. 長期効果と安全性(5年フォローアップ)
Kim et al. (2022)による5年間のフォローアップ研究では、以下の知見が得られています:
5年フォローアップの結果
- 効果の持続:疼痛・機能改善効果は5年後も一定程度維持されていた
- 安全性の確認:5年間の観察期間中、重篤な有害事象や腫瘍形成は認められず
- 放射線学的変化:一部の患者で関節症の進行抑制を示唆する所見
- 追加治療の必要性:一部の患者では効果減弱に伴い追加治療が検討された
3-5. メタアナリシスによる総合評価
複数の系統的レビューとメタアナリシスにより、脂肪由来幹細胞治療の有効性が支持されています:
- 疼痛改善:対照群と比較して統計学的に有意な疼痛軽減効果(標準化平均差 0.5-0.8)
- 機能改善:WOMAC機能スコア・KOOSスコアで有意な改善
- 安全性:重篤な有害事象の報告は稀で、全体的に安全性が高い
- 効果の持続性:6-12ヶ月以上の中長期的効果が確認されている
3-6. 作用機序の考察
脂肪由来幹細胞が変形性膝関節症に対して効果を示すメカニズムとして、以下が考えられています:
| 作用機序 | 具体的効果 |
|---|---|
| 抗炎症作用 | 炎症性サイトカイン(IL-1β、TNF-α)の抑制、抗炎症性サイトカイン(IL-10)の増加 |
| 軟骨保護作用 | 軟骨分解酵素(MMPs)の抑制、軟骨マトリックス成分の産生促進 |
| 組織修復促進 | 成長因子(TGF-β、IGF-1)の分泌による組織再生促進 |
| 血管新生促進 | VEGFの分泌により滑膜・軟骨下骨への血流改善 |
| 免疫調節作用 | 免疫細胞の活性調節により過剰な免疫反応を抑制 |
| 分化能 | 軟骨細胞への分化により軟骨組織の補充(程度は限定的) |
※Gimble et al. (2007)、Lee et al. (2019)より
臨床的有効性のまとめ:
大規模な無作為化比較試験により、脂肪由来幹細胞の関節内注射は変形性膝関節症の疼痛軽減と機能改善に有意な効果があることが実証されました(Lee et al., 2023)。効果は中長期的に持続し、重篤な副作用も報告されていません。ただし、軟骨の構造的な再生効果については今後の長期的な検証が必要です。治療適応や効果の程度については、個々の患者の病状・年齢・関節症の重症度などを考慮した総合的な判断が求められます。
4. 安全性と副作用
4-1. 大規模臨床試験における安全性データ
Lee et al. (2023)のPhase III試験(261例)および過去の複数の臨床試験において、脂肪由来幹細胞治療の安全性が検証されています。
主要な安全性の知見
- 重篤な有害事象:治療に関連した重篤な有害事象は報告されていない(Lee et al., 2019; Lee et al., 2023)
- 感染症:関節内注射に伴う感染症の発生率は対照群と同程度で非常に低い
- 腫瘍形成:5年間のフォローアップで腫瘍形成は認められず(Kim et al., 2022)
- 免疫反応:自家移植のため、重篤なアレルギー反応や免疫拒絶反応は報告されていない
- 全身性の副作用:関節内投与による全身性の副作用は極めて稀
4-2. 報告されている有害事象
| 有害事象 | 発生頻度 | 重症度 | 対処法 |
|---|---|---|---|
| 注射部位の疼痛・腫脹 | 10-20% | 軽度 | 数日以内に自然軽快、冷却・鎮痛薬で対応 |
| 一時的な関節内圧上昇感 | 5-10% | 軽度 | 数日で改善、安静で対応 |
| 脂肪吸引部の軽度疼痛 | 10-15% | 軽度 | 1-2週間で改善、鎮痛薬で対応 |
| 一時的な関節可動域制限 | 5%以下 | 軽度 | リハビリテーションで改善 |
| 感染症 | 1%未満 | 軽度~中等度 | 抗菌薬投与、必要に応じ洗浄 |
| アレルギー反応 | 1%未満 | 軽度 | 抗ヒスタミン薬、ステロイド投与 |
※Lee et al. (2019; 2023)、Kim et al. (2022)より
4-3. 長期安全性の検証
Kim et al. (2022)による5年間のフォローアップ研究では、長期的な安全性が確認されています:
- 腫瘍形成リスク:5年間の観察期間中、治療に関連した腫瘍形成は一例も報告されず
- 関節構造への影響:異所性骨化・石灰化などの異常な組織形成は認められず
- 全身への影響:血液検査・尿検査などで全身的な異常所見なし
- 追加治療の必要性:一部の患者で効果減弱により追加治療が行われたが、重篤な合併症なく施行可能
4-4. 禁忌と注意事項
治療が適さない場合(禁忌・慎重投与)
- 活動性感染症:関節内または全身の活動性感染症がある場合
- 悪性腫瘍の既往:活動性の悪性腫瘍または治療中の癌がある場合は慎重に判断
- 重度の出血傾向:抗凝固薬の使用中や血液凝固異常がある場合は注意が必要
- 妊娠・授乳中:安全性が十分に確立されていないため慎重に判断
- 自己免疫疾患:活動性の自己免疫疾患がある場合は医師と相談
- 重度の全身疾患:コントロール不良の糖尿病・心疾患などがある場合は慎重に判断
4-5. 品質管理と規制
臨床応用される脂肪由来幹細胞は、厳格な品質管理のもとで調製されます:
- GMP基準:Good Manufacturing Practice(医薬品製造管理基準)に準拠した施設で培養
- 細胞の純度:間葉系幹細胞マーカー(CD73、CD90、CD105)の発現確認
- 微生物検査:無菌試験・エンドトキシン試験により汚染がないことを確認
- 生存率:投与時の細胞生存率が一定基準(通常80%以上)を満たすことを確認
- 遺伝的安定性:培養過程での遺伝子変異がないことを確認
安全性のまとめ:
多数の臨床試験と5年間の長期フォローアップにより、自家脂肪由来幹細胞治療は高い安全性を持つ治療法であることが示されています(Lee et al., 2019; Lee et al., 2023; Kim et al., 2022)。重篤な副作用・腫瘍形成・免疫拒絶反応などの報告はなく、発生する有害事象の多くは軽度で一時的なものです。ただし、医療機関の選択においては、適切なGMP基準に準拠した施設で治療を受けることが重要です。治療を検討する際は、医師と十分に相談し、個々の健康状態に応じた適切な判断を行ってください。
大阪で頭痛の相談は、いわた脳神経外科クリニックへどうぞ。ご予約は、下記から可能です。
5. 今後の展望:老化関連疾患への応用拡大
5-1. 変形性関節症以外への応用可能性
脂肪由来幹細胞は変形性膝関節症での有効性が実証されていますが、その多面的な作用機序から、他の老化関連疾患への応用も期待されています。
研究が進行中の応用領域
- 心血管疾患:虚血性心疾患・心不全に対する血管新生促進・心筋保護作用(Gimble et al., 2007)
- 神経変性疾患:パーキンソン病・アルツハイマー病に対する神経保護・抗炎症作用
- 糖尿病合併症:糖尿病性潰瘍・神経障害に対する組織修復促進
- 皮膚老化:しわ・たるみに対するコラーゲン産生促進・皮膚再生
- 骨粗鬆症:骨形成促進・骨密度改善
- 腱・靭帯損傷:スポーツ外傷・変性に対する組織修復
5-2. 技術的進歩と治療最適化
脂肪由来幹細胞治療の効果を最大化するため、以下のような技術革新が進められています:
| 技術革新 | 内容 | 期待される効果 |
|---|---|---|
| 細胞のプライミング | 投与前に特定の成長因子で細胞を活性化 | 組織修復能・生着率の向上 |
| 遺伝子改変 | 特定の成長因子遺伝子を導入 | 治療効果の増強・持続化 |
| スキャフォールド技術 | 生体適合性素材と組み合わせて投与 | 細胞の生着率向上・組織構造の再建 |
| エクソソーム治療 | 幹細胞が分泌する小胞を利用 | 細胞移植なしでパラクリン効果を発揮 |
| 3D培養技術 | 立体的な環境で細胞を培養 | 細胞機能の向上・生体内環境の模倣 |
| バイオプリンティング | 3Dプリンターで細胞を配置 | 複雑な組織構造の再建 |
5-3. 個別化医療への展開
将来的には、患者個々の特性に応じた最適な幹細胞治療の提供が期待されています:
- バイオマーカーによる効果予測:治療前に効果が期待できる患者を選別
- 細胞品質の個別評価:患者由来細胞の機能を評価し、最適な培養条件を決定
- 投与法の最適化:疾患の種類・重症度に応じた投与量・投与経路の選択
- 併用療法の開発:他の治療法(リハビリ・薬物療法)との最適な組み合わせ
- 遺伝子プロファイリング:遺伝的背景に基づく治療反応性の予測
5-4. 規制と社会実装の課題
克服すべき課題
- 製造コスト:GMP基準の細胞培養施設運営には高額な費用が必要
- 保険適用:現時点では自由診療が主体で、患者負担が大きい
- 標準化:施設間での細胞調製・品質管理方法の統一が必要
- 長期効果の検証:構造的な組織再生効果については更なる長期データが必要
- 効果予測因子の同定:どのような患者に特に有効かの明確化
- 倫理的配慮:適応拡大に伴う倫理的課題への対応
5-5. アンチエイジング医療における位置づけ
脂肪由来幹細胞治療は、包括的なアンチエイジング医療の一翼を担う可能性があります:
統合的アンチエイジングアプローチ
- 疾患治療:老化関連疾患(関節症・心血管疾患など)の治療
- 予防医療:疾患発症前の早期介入による老化進行の抑制
- QOL向上:運動機能・認知機能の維持による生活の質向上
- 美容医療:皮膚の若返り・毛髪再生などの美容的効果
- 全身的アプローチ:代謝調節・炎症抑制による全身的な老化遅延
今後の展望のまとめ:
脂肪由来幹細胞治療は、変形性膝関節症での有効性実証を皮切りに、様々な老化関連疾患への応用拡大が期待されています。技術革新により治療効果の向上が見込まれ、個別化医療の実現により最適な治療提供が可能になるでしょう。一方で、製造コスト・保険適用・標準化などの課題も残されており、社会実装に向けた継続的な取り組みが必要です。将来的には、包括的なアンチエイジング医療の中核を担う治療法として、多くの患者さんのQOL向上に貢献することが期待されます。
6. よくある質問(Q&A)
Q1. 脂肪由来幹細胞治療はどのような人に適していますか?
A. 主に以下のような方が治療の対象となります。
適応となる可能性が高い方:
- 変形性膝関節症:保存的治療(内服・注射・リハビリ)で十分な効果が得られない中等度~重度の患者さん
- 活動性の高い方:スポーツや仕事で膝を使う機会が多く、人工関節手術を避けたい方
- 50-75歳程度:比較的若年で、長期的な関節機能維持を希望される方
- 全身状態良好:重篤な基礎疾患がなく、脂肪吸引・関節内注射が安全に実施できる方
慎重に判断が必要な方:
- 活動性の悪性腫瘍がある方
- 活動性の感染症がある方
- 重度の関節変形がある方(効果が限定的な可能性)
治療の適応については、画像検査(X線・MRI)と診察により、医師が総合的に判断いたします。
Q2. 治療の流れと期間はどのくらいですか?
A. 以下のような流れで治療が進行します。
治療の流れ:
- 初診・適応評価(1日目)
- 診察・画像検査(X線・MRI)による病状評価
- 治療の適応判断・リスク評価
- 治療内容・費用の説明
- 脂肪組織の採取(2日目、約1-2時間)
- 局所麻酔下で腹部または大腿部から脂肪吸引(約10-20ml)
- 日帰りまたは短時間の入院
- 細胞培養期間(約3-4週間)
- GMP基準の施設で幹細胞を培養・拡大
- 品質管理(純度・生存率・無菌性の確認)
- 関節内投与(3日目、約30分)
- 超音波ガイド下で膝関節内に細胞を注射
- 日帰り治療
- フォローアップ(定期通院)
- 投与後1ヶ月・3ヶ月・6ヶ月・12ヶ月時点で経過観察
- 効果判定・副作用のチェック
効果発現時期:多くの患者さんで投与後1-3ヶ月で疼痛軽減・機能改善を実感し、効果は6-12ヶ月以上持続する可能性が示唆されました(Lee et al., 2019; Lee et al., 2023)。
Q3. 治療後の生活制限はありますか?
A. 投与後の一定期間、軽度の制限があります。
投与直後~1週間:
- 安静:激しい運動・重労働は避け、日常生活動作は可能
- 関節への負担軽減:長時間の立位・歩行・階段昇降を控える
- 冷却:腫脹がある場合は関節を冷やす
1-4週間:
- 軽い運動から再開:ウォーキング・水泳など低負荷の運動から徐々に再開
- リハビリテーション:理学療法士の指導のもと、関節可動域訓練・筋力トレーニング
1ヶ月以降:
- 通常の活動:症状に応じて通常の活動レベルに戻す
- スポーツ:医師と相談の上、段階的に再開
個々の回復状況により制限期間は異なりますので、医師の指示に従ってください。
7. まとめ
- 脂肪由来幹細胞の特性
- 皮下脂肪から容易に採取でき、豊富な細胞数と高い増殖能を持つ
- 多分化能・パラクリン効果・免疫調節作用など多彩な治療効果を発揮(Gimble et al., 2007)
- 骨髄由来幹細胞と比較して、採取が低侵襲で患者負担が軽い
- 老化遅延のメカニズム
- ミトファジー促進により損傷ミトコンドリアを除去し、代謝恒常性を調節(Lv et al., 2021)
- 抗炎症作用・抗酸化作用により細胞老化を遅延
- 組織修復促進により老化に伴う組織変性を改善
- 臨床的有効性
- 変形性膝関節症に対するPhase III試験(261例)で有意な疼痛軽減・機能改善を実証(Lee et al., 2023)
- VAS疼痛スコア25.2点改善(p=0.004)、WOMAC総スコア21.7点改善(p=0.002)
- 効果は6-12ヶ月以上持続し、5年フォローアップでも安全性を確認(Kim et al., 2022)
- 高い安全性
- 重篤な治療関連有害事象・腫瘍形成・免疫拒絶反応の報告なし
- 発生する副作用の多くは軽度で一時的(注射部位の疼痛・腫脹など)
- 自家移植のため免疫学的リスクが低い
- 多様な応用可能性
- 変形性関節症以外にも、心血管疾患・神経変性疾患・糖尿病合併症などへの応用が研究中
- 技術革新(細胞プライミング・エクソソーム治療など)により効果向上が期待
- 包括的アンチエイジング医療の一翼を担う可能性
- 今後の課題
- 製造コスト・保険適用・標準化などの社会実装に向けた課題
- 長期的な構造再生効果の検証
- 効果予測因子の同定による個別化医療の実現
脂肪由来幹細胞治療は、老化に伴う疾患の新たな治療選択肢です。
大規模臨床試験により変形性膝関節症に対する有効性と安全性が実証され、さらにミトファジー促進による代謝調節を通じて、より広範な老化関連疾患への応用が期待されています(Lv et al., 2021; Lee et al., 2023)。
当院では、患者さんの病状・年齢・ライフスタイルを総合的に評価し、適切な治療選択肢をご提案いたします。脂肪由来幹細胞治療は、必要に応じて高度医療機関と連携して実施いたします。
膝の痛みや老化に伴う体の衰えでお悩みの方は、お気軽にご相談ください。専門医が丁寧に診察し、最適な治療計画をご提案いたします。
お問い合わせ・ご予約
大阪市で再生医療・幹細胞治療の相談なら、いわた脳神経外科クリニックへどうぞ。ご予約は、下記から可能です。
当院では、皆様の悩みにしっかり寄り添います。また当院公式LINEにてご質問等をお受けしておりますので、お気軽にお問い合わせくださいませ。
様々な治療に関する記事はこちら
自家がんワクチンについて
脳腫瘍の摘出手術前
参考文献
- Gimble, J.M., Katz, A.J. and Bunnell, B.A. (2007) ‘Adipose-derived stem cells for regenerative medicine’, Circulation Research, 100(9), pp. 1249-1260. doi: 10.1161/01.RES.0000265074.83288.09.
- Kim, K.I., Lee, W.S., Kim, J.H., Bae, J.K. and Jin, W. (2022) ‘Safety and efficacy of the intra-articular injection of mesenchymal stem cells for the treatment of osteoarthritic knee: a 5-year follow-up study’, Stem Cells Translational Medicine, 11(6), pp. 586-596. doi: 10.1093/stcltm/szac028.
- Lee, W.S., Kim, H.J., Kim, K.I., Kim, G.B. and Jin, W. (2019) ‘Intra-articular injection of autologous adipose tissue-derived mesenchymal stem cells for the treatment of knee osteoarthritis: a phase IIb, randomized, placebo-controlled clinical trial’, Stem Cells Translational Medicine, 8(6), pp. 504-511. doi: 10.1002/sctm.18-0122.
- Lee, W.S., Kim, H.J., Kim, K.I., Kim, G.B. and Jin, W. (2023) ‘Clinical efficacy and safety of the intra-articular injection of autologous adipose-derived mesenchymal stem cells for knee osteoarthritis: a phase III, randomized, double-blind, placebo-controlled trial’, The American Journal of Sports Medicine, 51(9), pp. 2243-2253. doi: 10.1177/03635465231179223.
- Lv, M., Zhang, S., Guo, S., Jiang, B., Cao, L., Cao, S. and Dong, Y. (2021) ‘Adipose-derived stem cells regulate metabolic homeostasis and delay aging by promoting mitophagy’, The FASEB Journal, 35(7), e21675. doi: 10.1096/fj.202100332R.