【結論】腫瘍悪性度の予測マーカーと新たな組成物の発見が、膠芽腫治療の未来を拓く
1. 予測マーカーの重要性: 治療抵抗性を持つ「がん幹細胞(CSCs)」を特定・標的とするために、精度の高いマーカーが不可欠です。
2. 新たなマーカーの発見: 膠芽腫(グリオブラストーマ)において、MSMPやICOSLGといった特有のタンパク質が高い悪性度や予後不良と関連していることが解明されています。
3. 免疫逃避メカニズムの解明: ICOSLGは、免疫を抑制するT細胞(IL-10産生)を増殖させ、腫瘍が免疫系から逃れる手助けをしていることが分かりました。
4. 窒素含有化合物への期待: これらのマーカーを標的とする「窒素含有化合物およびそれを含む組成物」の研究が進められており、新たな治療薬・診断薬としての可能性が期待されています。
5. 個別化医療の進歩: 患者さんごとの腫瘍の特性(マーカー)を分析し、将来的にはより効果的で副作用の少ない治療戦略が選択できるようになる展望があります。
「悪性の脳腫瘍と診断されたが、今の治療で本当に再発を防げるのだろうか…」「現在の医学研究はどこまで進んでいるのか知りたい」—そんな切実な思いを抱えていらっしゃいませんか?
最も悪性度が高いとされる脳腫瘍である膠芽腫(グリオブラストーマ:GBM)は、手術や放射線治療、化学療法を組み合わせた集学的治療を行っても、生存期間中央値は約14.6ヶ月とされており、再発率が高く、治療が非常に難しい疾患として知られています(Maruyama et al., 2021)。しかし現在、日本の医学研究グループによって「腫瘍の悪性度を予測する新たなマーカー」や、それらを標的とする「窒素含有化合物を含む組成物」の開発など、希望に繋がる研究が日々進められています。
膠芽腫の治療課題と研究の焦点
- がん幹細胞の存在: 再発の主な原因は、従来の治療に抵抗性を示す「がん幹細胞(CSCs)」の存在だと考えられています。
- 新たなマーカーMSMP: がん幹細胞モデルにおいて非常に高く発現する遺伝子(MSMP)が特定されました。
- 免疫を抑制するICOSLG: 特に悪性度の高い「間葉系(MES)」の膠芽腫において、ICOSLGという分子が強く発現し、予後不良と関連することが判明しました(Iwata et al., 2020)。
- → 注目される特許技術: これらの予測マーカーを活用した「窒素含有化合物を含む組成物」が新たな診断・治療のアプローチとして注目されています。
本記事では、医学論文および特許情報に基づき、腫瘍悪性度の予測マーカーの役割と、未来の治療薬として期待される窒素含有化合物・組成物の展望について、専門的かつ分かりやすく解説します。
この記事で分かること
・がん幹細胞(CSCs)とは: 膠芽腫の再発要因と治療の壁
・新たな悪性度予測マーカー: MSMPとICOSLGの発見とその働き
・腫瘍の免疫逃避: がん細胞が免疫から隠れる巧妙なメカニズム
・未来の治療組成物: 「窒素含有化合物」がもたらす可能性
・現在の治療の限界と展望: 個別化医療へ向けたステップ
・よくある質問: 患者さんやご家族の疑問に専門医視点で回答
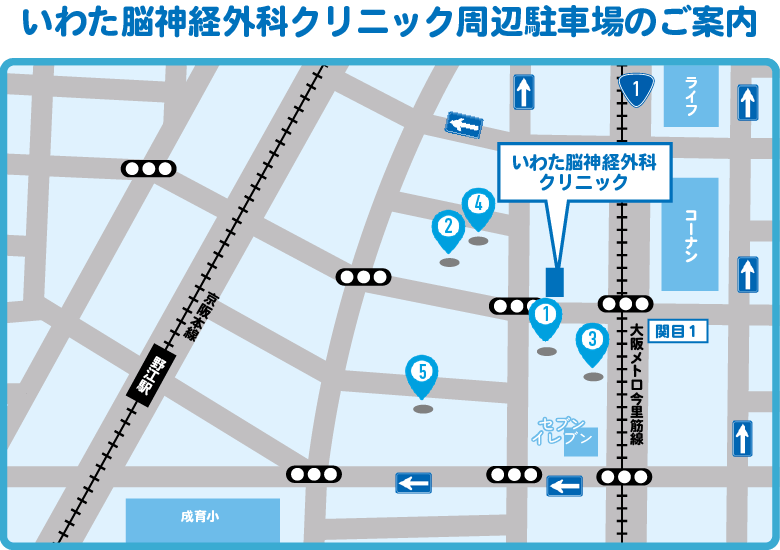
大阪で脳腫瘍・脳の病気の相談なら、いわた脳神経外科クリニックへどうぞ。ご予約は、下記から可能です。
全国からのご来院があります。もちろん近隣(大阪市生野区や大阪上本町など)からも歓迎しております。
目次
1. 膠芽腫とがん幹細胞(CSCs)の課題
1-1. 膠芽腫(GBM)の難治性
膠芽腫(GBM)は、原発性脳腫瘍の中で最も発生頻度が高く、かつ悪性度が高い腫瘍です。手術、放射線療法、化学療法を用いた集学的治療を行っても、診断からの生存期間中央値は約14.6ヶ月とされており、非常に厳しい現実があります。(Stupp et al. 2009)
1-2. なぜ再発を繰り返すのか?
- がん幹細胞(CSCs)の存在: 腫瘍細胞の中にごくわずかに存在する「がん幹細胞」が、再発の主な原因と考えられています。
- 治療抵抗性: これらの幹細胞は、従来の抗がん剤や放射線治療に対して強い抵抗性を持ち、治療後も生き残って再び腫瘍を形成します。
- 不均一性: がん幹細胞自体にも多様性(不均一性)があり、単一の治療法ですべてを死滅させるのが困難です。
2. 腫瘍悪性度の予測マーカー(MSMPとICOSLG)
治療が難しいがん幹細胞を特定し、ピンポイントで攻撃するためには、「予測マーカー」の発見が鍵となります。これまでの研究で、2つの極めて重要なマーカーが注目されています。
2-1. 幹細胞マーカー「MSMP」
Maruyama et al. (2021) の研究では、膠芽腫の細胞から「がん幹細胞モデル(P4E8細胞)」を樹立し、その遺伝子を解析しました。その結果、元の細胞と比較して最も高く発現していた遺伝子がMSMP(PC3分泌マイクロプロテイン)でした。
- MSMPは患者さんの膠芽腫組織において、グレード(悪性度)を問わずタンパク質レベルで発現していることが確認されました。
- このMSMPが、腫瘍の発生や進行(悪性化)に深く関与している可能性が示唆されています。
2-2. 免疫逃避を促すマーカー「ICOSLG」
もう一つの重要な発見が、ICOSLG(誘導性T細胞共刺激リガンド)です。Iwata et al. (2020) の研究によると、ICOSLGは膠芽腫の中でも特に悪性度の高い「間葉系(MES)がん幹細胞」で強く発現していることが分かりました。
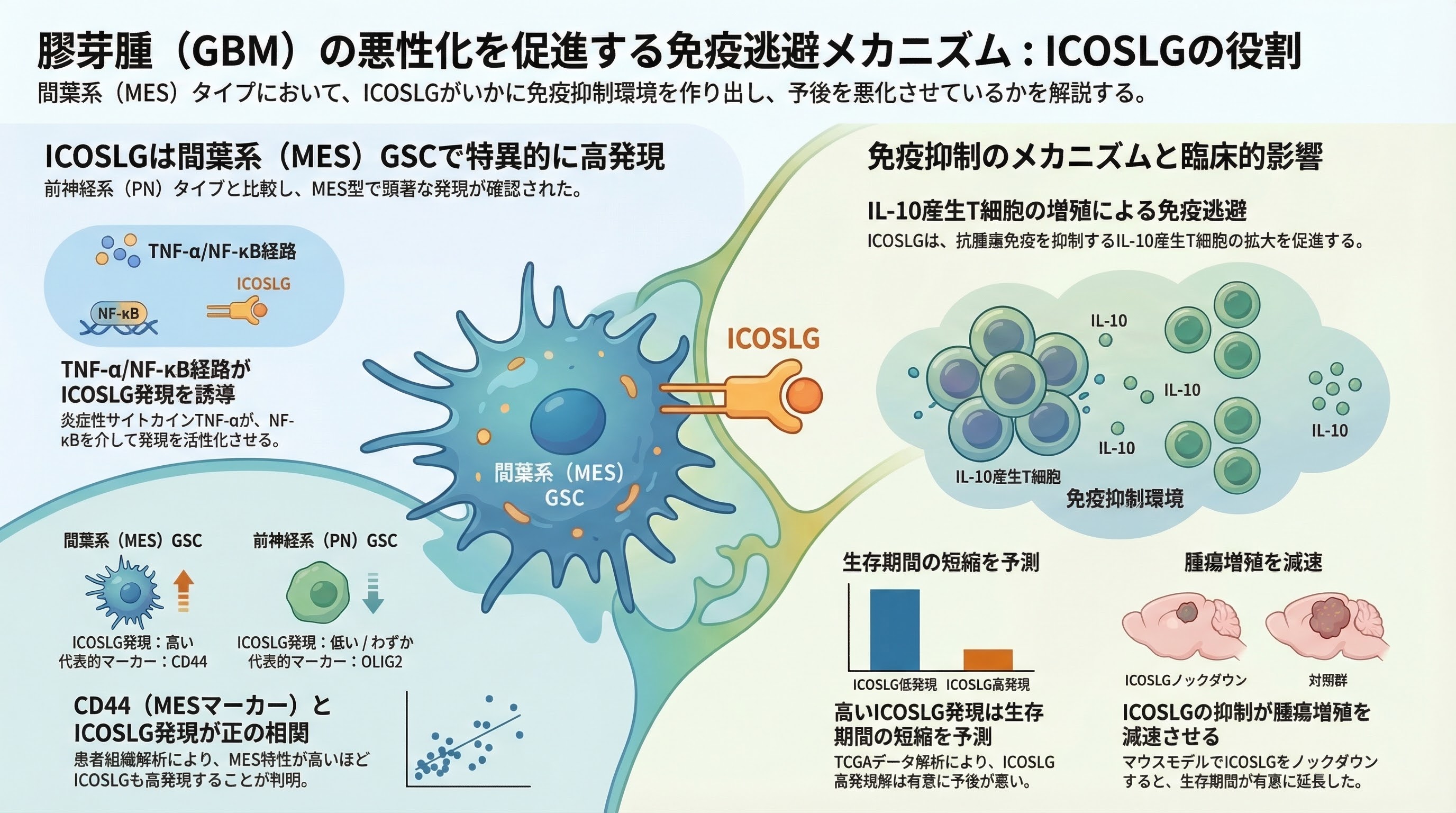
2-3. ICOSLGがもたらす「免疫のブレーキ」
- IL-10産生T細胞の増加: ICOSLGが発現すると、免疫を抑え込む働きを持つ「IL-10(インターロイキン-10)」を産生するT細胞が増加します。
- 予後への影響: 臨床データでも、このICOSLGの発現が高い患者さんほど、予後が不良であることが示されています。
- 治療への期待: 逆に言えば、このICOSLGの遺伝子を抑え込む(ノックダウンする)と、免疫が正常に働き、マウスのモデル実験では腫瘍の成長が著しく抑制されました。
大阪で脳腫瘍・脳の病気の相談なら、いわた脳神経外科クリニックへどうぞ。ご予約は、下記から可能です。
3. 新たな組成物「窒素含有化合物」への期待
上記のような画期的なマーカー(MSMPやICOSLG)の解明を受け、それらを利用・標的とする全く新しい治療法や診断薬の研究が進んでいます。その最前線にあるのが、Hayashi et al. (2024) らによる「窒素含有化合物、前記窒素含有化合物を含む組成物、及び腫瘍悪性度の予測マーカー」に関する技術(特許WO2024075736A1)です。
3-1. 窒素含有化合物の組成物が意味するもの
現在、特許出願および研究が進められている技術ですが、以下のような展開が期待されています。
- 高精度な診断薬としての応用: 特殊な「窒素含有化合物」を用いることで、腫瘍の悪性度マーカーを迅速かつ正確に検知する組成物が開発されれば、患者さんごとの腫瘍の性質(悪性度やタイプ)を早期に見極められるようになります。
- 標的治療薬としての可能性: がん幹細胞特有の経路や、免疫逃避を促す経路(ICOSLGなど)を阻害するための化合物の基盤となり得ます。
3-2. 個別化医療(プレシジョン・メディシン)の実現へ
これまでの「全てのがんに同じ抗がん剤を使う」アプローチから、「予測マーカーを用いて、特定の標的を持つ患者さんにだけ、特効性のある組成物(薬)を投与する」という、副作用を抑えつつ効果を最大化する個別化医療へのシフトが進んでいます。今回挙げた新しい化合物やマーカーは、その重要なピースとなります。
【個別化治療】患者個人へのオーダーメイド治療:自家がんワクチン
4. 現状の治療の限界と今後の展望
新しい発見がある一方で、乗り越えなければならない医療の壁も存在します。
| 現在の課題 | 今後の展望と対策 |
|---|---|
| 血液脳関門(BBB)の壁 脳を守る関門が、薬の到達も妨げてしまう。 |
新しい窒素含有化合物や組成物の最適化により、脳内への移行性を高めるドラッグデリバリーシステムの開発が進んでいます。 |
| がん幹細胞の多様性 単一のマーカーだけでは全ての幹細胞を叩けない。 |
MSMPやICOSLGなど複数のマーカーを同時に評価し、複数の治療薬を組み合わせる併用療法が模索されています。 |
| 免疫療法の副作用 免疫を活性化しすぎると自己免疫疾患に似た副作用が出る。 |
悪性度マーカーに基づく精密な投与量の調整や、副作用を抑制する支持療法との併用が進化しています。 |
5. よくある質問(Q&A)
Q1. 腫瘍の悪性度マーカーがわかると、治療はどう変わりますか?
A. より適切で無駄のない治療法(個別化医療)の選択が可能になります。
腫瘍がどのマーカー(例えばICOSLGやMSMPなど)を持っているかが事前に判明すれば、効かない可能性が高い治療を避け、効果が期待できる分子標的薬や免疫療法をピンポイントで選ぶことができるようになります。これにより、副作用の軽減と生存期間の延長が期待されます。
Q2. 紹介された新しい「窒素含有化合物」の薬はいつ治療に使えますか?
A. 現在は研究・特許出願の段階であり、実用化にはもう少し時間がかかります。
新しい組成物や化合物が実際の医療現場で使えるようになるためには、細胞実験、動物実験を経て、安全性を確かめる臨床試験(治験)をクリアする必要があります。数年〜十数年の期間を要しますが、着実に次世代の治療の種は育っています。
Q3. MSMPやICOSLGといったマーカーは、現在一般的な検査で調べられますか?
A. 標準的な健康診断や一部の病院では、まだルーチンには組み込まれていません。
これらは先行研究で特定されたマーカーであり、主として大学病院などの研究機関において、遺伝子パネル検査等を通じて調べられる場合があります。将来的に、特許技術である診断用組成物が実用化されれば、より手軽に検査できるようになる可能性があります。
Q4. 膠芽腫(グリオブラストーマ)の再発を防ぐ方法はありますか?
A. 現在の医学では完全な再発予防は困難ですが、様々なアプローチが試みられています。
手術で可能な限り腫瘍を摘出した後、放射線と化学療法(テモゾロミドなど)を組み合わせるのが標準治療です。それに加え、現在では腫瘍治療電場療法(TTFields)や、免疫の力を利用する自家がんワクチンなどの臨床研究も進んでおり、これらの集学的アプローチで再発を少しでも遅らせる努力が行われています。
6. まとめ
- がん幹細胞研究の重要性
- 膠芽腫の再発の根源であるがん幹細胞(CSCs)を標的とした研究が加速しています。
- 新たな悪性度予測マーカーの発見
- MSMPタンパク質やICOSLG分子が、膠芽腫の悪性度と深く関連していることが証明されました(Maruyama et al., 2021; Iwata et al., 2020)。
- 腫瘍の免疫逃避メカニズム
- ICOSLGは免疫を抑制するT細胞を増やし、がんが体内で生き延びる手助けをしています。これを防ぐことが新しい治療の糸口となります。
- 窒素含有化合物への期待
- これらのマーカーに基づく新しい「窒素含有化合物とその組成物」の開発は、次世代の個別化医療を担う技術として特許が出願され、世界から注目されています(Hayashi et al., 2024)。
医学は日々進歩し、希望の光は確実に広がっています。
悪性脳腫瘍という厳しい診断を受けたとしても、これまでの医学研究は細胞レベル・遺伝子レベルでその弱点を解き明かしつつあります。新しい予測マーカーやそれを用いた組成物の研究は、「効く薬を、効く人にピンポイントで届ける未来」を約束するものです。
当院では、専門知識に基づいた客観的かつ正確な情報をご提供するとともに、患者さんの心に寄り添った診療を心がけております。頭部の症状に不安がある方、また今後の治療動向について相談したい方は、一人で悩まず専門医にぜひご相談ください。
さらに、標準治療に加え、患者さん自身の免疫を活性化させる治療選択肢にも注目が集まっています。膠芽腫に対する自家がんワクチン療法などもその一つであり、自家がんワクチン療法について詳しくはこちらをご覧ください。
お問い合わせ・ご予約
脳腫瘍・脳の病気の相談なら、いわた脳神経外科クリニックへどうぞ。ご予約は、下記から可能です。
当院では、皆様の悩みにしっかり寄り添います。また当院公式LINEにてご質問等をお受けしておりますので、お気軽にお問い合わせくださいませ。
脳腫瘍関連記事はこちら
参考文献
- Hayashi, M., Ikeda, K. and Iwata, R. (2024) ‘WO2024075736A1: 窒素含有化合物、前記窒素含有化合物を含む組成物、及び腫瘍悪性度の予測マーカー’, World Intellectual Property Organization. Available at: https://jglobal.jst.go.jp/detail?JGLOBAL_ID=202503002261413720
- Iwata, R., Lee, J.H., Hayashi, M., Dianzani, U., Ofune, K., Maruyama, M., Oe, S., Ito, T., Hashiba, T., Yoshimura, K., Nonaka, M., Nakano, Y., Norian, L., Nakano, I. and Asai, A. (2020) ‘ICOSLG-mediated regulatory T-cell expansion and IL-10 production promote progression of glioblastoma’, Neuro-Oncology, 22(3), pp. 333-344. doi: 10.1093/neuonc/noz204.
- Maruyama, M., Nakano, Y., Nishimura, T., Iwata, R., Matsuda, S., Hayashi, M., Nakai, Y., Nonaka, M. and Sugimoto, T. (2021) ‘PC3-Secreted Microprotein Is Expressed in Glioblastoma Stem-Like Cells and Human Glioma Tissues’, Biological and Pharmaceutical Bulletin, 44(7), pp. 910-919.
- Stupp, R., Hegi, M.E., Mason, W.P., van den Bent, M.J., Taphoorn, M.J., Janzer, R.C., Ludwin, S.K., Allgeier, A., Fisher, B., Belanger, K., Hau, P., Brandes, A.A., Gijtenbeek, J., Marosi, C., Vecht, C.J., Mokhtari, K., Wesseling, P., Villa, S., Eisenhauer, E., Gorlia, T., Weller, M., Lacombe, D., Cairncross, J.G. and Mirimanoff, R.O. (2009) ‘Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial’, The Lancet Oncology, 10(5), pp. 459-466. doi: 10.1016/S1470-2045(09)70025-7.